Madrid, 3 feb (EFE).- Los macrófagos, los centinelas del sistema inmunitario que nos defienden de los microbios y regulan el buen funcionamiento de los tejidos y de la inflamación, adaptan sus necesidades metabólicas al órgano en el que se encuentran.
Así lo ha detallado una investigación del Centro Nacional de Investigaciones Cardiovasculares (CNIC) publicada este viernes en la revista Immunity.
El hallazgo permite entender mejor cómo el macrófago regula su metabolismo en función del órgano en el que reside y aporta información valiosa sobre la vulnerabilidad de estas células que contribuyen a las enfermedades inflamatorias crónicas.
Toda esta información se podría explotar terapéuticamente para tratar patologías asociadas a la obesidad y al síndrome metabólico, y también a las enfermedades cardiovasculares, según los autores.
Los macrófagos son células del sistema inmunitario que se encuentran repartidas por todos los tejidos y limpian el organismo de cualquier tipo de material biológico desechable, desde partículas nocivas como microcristales o virus, a proteínas o complejos más grandes que aparecen durante el desarrollo.
Pero también son importantes para regular el buen funcionamiento de la inflamación, un proceso que ayuda a reparar los tejidos y que si no se realiza correctamente conduce a la inflamación crónica que es el origen de muchas patologías como el síndrome metabólico asociado a la obesidad, la diabetes tipo 2 o las enfermedades cardiovasculares.
El trabajo del CNIC desvela que los macrófagos adaptan su metabolismo celular y su función al órgano donde residen.
"En los tejidos ricos en grasa y colesterol extracelular, como el pulmón o el bazo, los macrófagos acomodan su metabolismo y adquieren otro más específico dependiente de la actividad mitocondrial para degradar estas grasas a través de la respiración mitocondrial" dice Stefanie Wculek, primera autora del artículo.
En estos tejidos, "los macrófagos dependen de la actividad de respiración mitocondrial y, si se interfiere genética o farmacológicamente con dicha actividad, los macrófagos mueren en el pulmón o bazo, pero sobreviven en otros órganos donde no tienen esta dependencia metabólica", explica.
Por ejemplo, los macrófagos que se encuentran en la grasa corporal o el tejido adiposo de personas delgadas no están afectados por mitocondrias disfuncionales, pero en las personas obesas, el exceso de grasa hace que los macrófagos se activen y se conviertan en células inflamatorias que promueven el desarrollo de resistencia a la insulina, diabetes tipo 2 y el hígado graso.
Y es que, tal y como ha descubierto esta investigación, "los macrófagos dependen de la respiración mitocondrial para procesar este exceso de grasa lo que les hace vulnerables a intervenciones terapéuticas, como la inhibición farmacológica de este proceso de respiración mitocondrial", dice David Sancho, líder del laboratorio de Inmunobiología del CNIC y responsable del estudio.
Por tanto, subraya el investigador, hemos visto que "la inhibición de la respiración mitocondrial en estos macrófagos proinflamatorios causa su muerte y esto previene el desarrollo de obesidad, diabetes tipo 2 e hígado graso (síndrome metabólico) en un modelo experimental preclínico en ratón".
El hallazgo abre la puerta hacia una nueva vía terapéutica para algunas enfermedades asociadas a la obesidad y síndrome metabólico, como son las enfermedades cardiovasculares, concluyen los investigadores.
Una nueva diána terapéutica para tratar enfermedades asociadas a la obesidad

Una nueva diána terapéutica para tratar enfermedades asociadas a la obesidad. EFE.














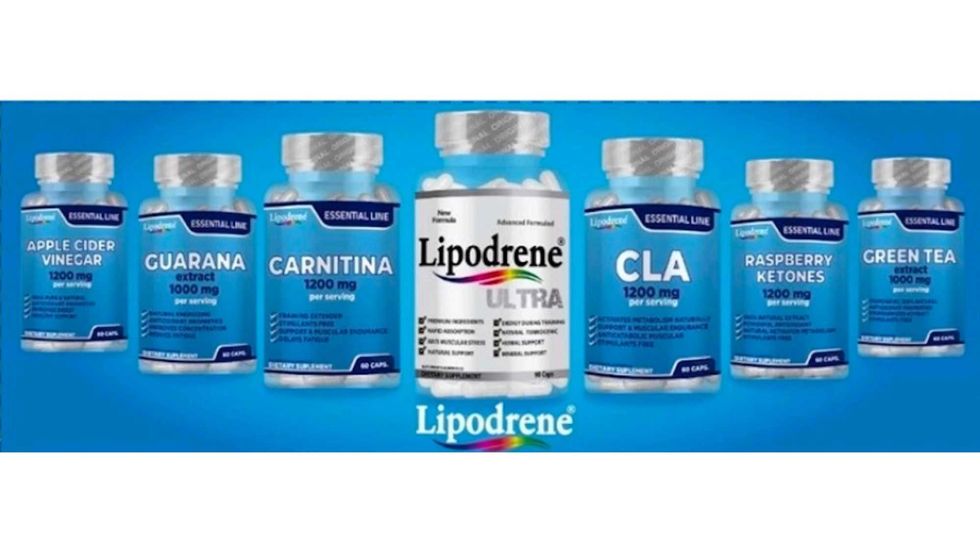 La SESA Querétaro difundió la alerta sanitaria emitida por Cofepris sobre dos líneas del suplemento Lipodrene.
La SESA Querétaro difundió la alerta sanitaria emitida por Cofepris sobre dos líneas del suplemento Lipodrene.